 On attribue généralement au philosophe grec Démocrite l’idée que la matière soit composée d’éléments plus ou moins indivisibles : les atomes. Si l’idée était juste, Démocrite n’avait pas réalisé à l’époque à quel point les atomes qui nous entourent sont petits : moins d’un nanomètre, soit un milliardième de mètre !
On attribue généralement au philosophe grec Démocrite l’idée que la matière soit composée d’éléments plus ou moins indivisibles : les atomes. Si l’idée était juste, Démocrite n’avait pas réalisé à l’époque à quel point les atomes qui nous entourent sont petits : moins d’un nanomètre, soit un milliardième de mètre !
Il a fallu ensuite attendre la fin du XIXème siècle pour que les physiciens apportent une preuve définitive de l’existence des atomes, et arrivent à estimer leur taille de manière suffisamment précise.
Et pourtant en 1762, Benjamin Franklin fit une observation étonnante qui aurait pu lui permettre un siècle avant tout le monde de réaliser à quel point les atomes et les molécules qui nous entourent sont petits. Mais bizarrement, il n’a pas poussé son raisonnement assez loin.
L’expérience de Franklin
 Rappelons tout d’abord qui était Benjamin Franklin, dont vous pouvez admirer la bouille sur les billets de 100$. Né en 1706 à Boston, il fut l’un des pères fondateurs des États-Unis d’Amérique, et co-auteur avec Thomas Jefferson de la déclaration d’indépendance de 1776.
Rappelons tout d’abord qui était Benjamin Franklin, dont vous pouvez admirer la bouille sur les billets de 100$. Né en 1706 à Boston, il fut l’un des pères fondateurs des États-Unis d’Amérique, et co-auteur avec Thomas Jefferson de la déclaration d’indépendance de 1776.
Ce fut donc un homme d’état d’exception, mais aussi un brillant physicien et inventeur. Il est d’ailleurs surtout connu pour sa célèbre et dangereuse expérience du cerf-volant, qui lui permit de démontrer la nature électrique de la foudre, et d’inventer le paratonnerre.
L’expérience dont je veux vous parler aujourd’hui n’est pas aussi connue que celle du cerf-volant, et pourtant à mon goût bien plus révolutionnaire !
En 1762, Franklin se promène au bord de l’étang de Clapham en Angleterre, et décide – allez savoir pourquoi ! – de verser un peu d’huile dans l’eau. Il observe alors qu’une tache se forme à la surface, et s’étend rapidement jusqu’à couvrir presque un quart de la superficie du plan d’eau.
Pour les anglophones, voici ce qu’il écrivait en 1773 à propos de cette observation :
“At length at Clapham where there is, on the common, a large pond, which I observed to be one day very rough with the wind, I fetched out a cruet of oil, and dropped a little of it on the water. I saw it spread itself with surprising swiftness upon the surface. The oil, though not more than a teaspoonful, produced an instant calm over a space several yards square, which spread amazingly and extended itself gradually until it reached the leeside, making all that quarter of the pond, perhaps half an acre, as smooth as a looking glass.”
Pour ceux que l’anglais rebute, l’essentiel est dans l’image ci-dessous, qui montre l’étang de Clapham avant et après y avoir déposé une goutte d’huile : observez le film d’huile, qui a comme propriété de « calmer » l’eau en rendant sa surface plus lisse et sans ondulations.
Quelle est l’épaisseur du film de l’huile ?
Ce qu’il y a de fascinant dans cette expérience, c’est qu’une si petite quantité d’huile (l’équivalent d’une cuillère d’après Franklin) puisse s’étaler sur une surface si grande : un demi-acre, ce qui fait environ 2000m2 dans nos unités. De manière assez incroyable, il semble que Benjamin Franklin n’ait pas pris la peine d’essayer de calculer l’épaisseur du film d’huile. Ca n’est qu’en 1890 que Rayleigh reprit l’expérience de Franklin et en déduisit cette épaisseur : et pourtant le calcul est élémentaire, et le résultat est sidérant !
Voyons cela : Franklin verse l’équivalent d’une cuillère d’huile, disons 2 cm3. Si le film s’étale sur 2000 m2, une simple division nous montre que celui-ci doit avoir une épaisseur d’environ…1 nanomètre ! Soit environ la taille d’une molécule d’huile. Sans le savoir, Benjamin Franklin était en train d’observer un film d’huile dont l’épaisseur n’était que d’une molécule. (Au passage, un truc bien plus fin que ce que je racontais dans ce billet sur les anneaux de Saturne !)
En faisant ce calcul tout simple, Franklin aurait pu conclure que les éléments qui composent la matière doivent être au moins aussi petits qu’un nanomètre. Au passage, il aurait également pu estimer le nombre de molécules présentes dans sa goutte d’huile et trouver quelque chose assez proche de l’énormité du nombre d’Avogadro, soit de l’ordre de 10^23.
Mais non, Franklin n’a pas eu l’idée de faire la division, et il a fallu attendre 100 ans plus tard, en 1865, pour que Johann Loschmidt estime par un autre moyen la taille des molécules de l’air, et que l’on réalise à quel point le monde atomique est petit…
L’expérience de Franklin chez vous
J’ai découvert que l’expérience de Franklin est au programme de physique du lycée, et que l’on peut la réaliser assez facilement en TP. Il vous faut pour cela un grand récipient rempli d’eau, du talc saupoudré en surface pour visualiser le film, et une goutte d’huile. Et voici ce que ça donne :
[dailymotion id=x6wuah]
Bon moi j’ai essayé dans ma cuisine, en remplaçant il est vrai le talc par du curry, et ça n’a pas marché ! La goutte ne s’étale pas 🙁 … probablement à cause de la présence de graisse résiduelle dans mon récipient, ou bien apportée par le curry lui-même. Mais ceux qui me connaissent savent que je suis un piètre expérimentateur !
Si certains ont eu cette expérience en TP, je suis curieux de connaitre leur réaction : pour ma part je la trouve absolument sidérante ! Mais je ne sais pas si à l’époque du lycée, assis au fond d’une salle de TP, j’aurais été frappé par le merveilleux de la chose !
Pour aller plus loin…
Pour ceux que ça intéresse, il faut savoir que l’histoire ne s’arrête pas là. Suite à la reprise de l’expérience de Franklin par Rayleigh, une série de physiciens ont continué à réaliser des films composés d’une ou plusieurs mono-couches de molécules d’huile. Le plus connu est Irving Langmuir, qui travailla chez General Electric avec Katherine Blodgett, et reçu le prix Nobel en 1932 pour ses contributions. On leur doit notamment une méthode permettant de déposer des monocouches sur une surface solide, en la trempant dans un liquide à la surface de laquelle flotte justement une moncouche d’huile. Le schéma ci-dessous (merci Wikipédia) montre le principe de cette méthode :

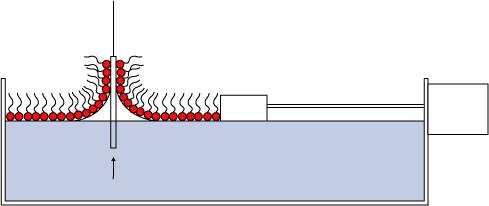




26 Comments
Joli petit billet.
Sais-tu si Franklin était sensibilisé à la théorie atomique ? Dans l’article sur B. Franklin, wikipedia.fr est ambigüe sur le sujet et wikipedia.en semble ne pas parler de cette expérience.
Je ne sais pas si j’ai été clair mais il me semblait que la théorie atomique était loin d’être admise à l’époque. C’était l’objet de ma question.
Ah effectivement je ne sais pas quel était le statut de la théorie atomique à l’époque. Mais même sans une telle théorie, calculer que la couche d’huile faisait 1 milliardième de mètre eut été déjà un choc !
J’ai eu cette expérience il y a deux ans en TP au collège (=lycée) en Suisse. Ça m’a vraiment impressionné et je voulais te conseiller de faire un article dessus ! Mais je ne l’ai finalement pas fait, par oubli probablement…
Et je me rappelle pas que Benjamin Franklin n’avait pas calculé l’épaisseur d’une molécule, il me semble que mon professeur disait qu’il avait justement pu calculer cette épaisseur.
Le verre float n’est pas très loin, une nappe de verre chaud qui s’étale sur de l’étain liquide.
Mon livre préféré sur cette physique :
« Gouttes,bulles,perles et ondes » de Pierre-Gilles de Gennes etal. Il y a même un cdrom avec des manips !
Excellent ce blog, je vais etre fan !
Très belle vulgarisation! En tant qu’enseignant de mathématique au niveau secondaire (équivalent du lycée, au Québec), j’utiliserai cet exemple pour expliquer la notion de figures et solides équivalents.
Bien que certains articles sont de trop haut niveau pour moi, j’apprécie toujours ce que je viens lire sur Science étonnante et je ne cesse d’apprendre. Continuez votre bon travail!
P.S. : Toujours à Boston?
Toujours à Boston, pour quelques années 8
C’est peut-être du pinaillage mais, Franklin pouvait-il savoir que le volume de la tâche et le volume de la cuillère étaient égaux ?
Autrement dit, la physique de son époque lui permettait-il de savoir que la tâche qu’il observait n’était composée que de l’huile de la cuillère ?
J’ai l’impression que oui. Il avait compris que la foudre c’est de l’électricité, alors j’imagine que l’étalement d’une tache d’huile est moins subtil comme notion. Mais c’est toujours difficile de se mettre dans la tête des gens d’un autre siècle 8
Merci, grâce à toi j’ai pu terminer et (enfin) comprendre mon exercices!
(Je crois que ça fait plus d’une demie heure que je suis dessus 😅)
Merci pour cet article particulièrement intéressant !
http://www.youtube.com/watch?v=rmSV2l6JFt0&feature=fvwrel
Je ne sais pas quand tous ça a été écrit juste pour une expérience sympas concernant le principe de la monocouche. Il faut prendre un fil de coton immaculé de graisse solide, Formé une boucle et le déposé à la surface de l eau contenu dans un récipient. Verser quelque goutte d huile dans la boucle, celle ci vas devenir circulaire et vous aurait un sorte de radeau d huile à la surface de l eau c est plutôt étonnant.
Bonjour,
L’expérience marche bien,mais il faut diluer l’huile dans un solvant volatil (acétone) pour que la monocouche se forme, du coup calcul supplémentaire.
Pingback: Gare au gorille ! | Physique à Main Levée
Bonjour,
J’aimerais savoir d’où proviennent les photographies montrant le lac avant et après y avoir déposé la goutte d’huile.
J’aurais dû mentionner la réf.
Elles viennent de là :
http://www.rsc.org/learn-chemistry/content/filerepository/CMP/00/000/687/isms-9.pdf?v=1399160447243
merci beaucoup
La goutte d’Huile qui couvre la surface d’une étendue d’eau, étonnant !
Les molécules sont vraiment fort mais pas assez bien plus simple
Enseignant de physique, mes élèves de seconde réalisent chaque année l’expérience dans un cristallisoir.
Le pb. est qu’il faut très peu de talc et utiliser de l’acide oléïque dilué dans de l’acétone.
Malheureusement, beaucoup d’élèves ont un niveau de math tellement mauvais qu’ils n’arrivent pas à exploiter eux mêmes leurs résultats.
Quel est le calcule ?
Pingback: Trois gouttes d’huile | La Forêt des Sciences
bonjour, je suis un étudiant et j’aimerais utiliser cette article. Je vous demande donc si les droit d’auteur son libre ?
Pingback: Lecture des pneus, pression et suspensions «