C’est l’été ! Et comme à la radio, j’en profite pour rediffuser quelques anciens épisodes. Certains récents, d’autres moins ! On commence avec celui-ci sur le bisphénol A et son étrange toxicité…
 Pas une semaine ne se passe sans que ne sorte une étude concernant le bisphénol A. Et bien sûr, si la plupart des études concluent à sa dangerosité, il s’en trouve une de temps en temps pour affirmer que sa toxicité est finalement limitée. Alors, toxique ou pas, le bisphénol A ?
Pas une semaine ne se passe sans que ne sorte une étude concernant le bisphénol A. Et bien sûr, si la plupart des études concluent à sa dangerosité, il s’en trouve une de temps en temps pour affirmer que sa toxicité est finalement limitée. Alors, toxique ou pas, le bisphénol A ?
Je me souviens d’avoir lu une fois que ces résultats en apparence contradictoires provenaient du fait que le bisphénol A est plus toxique à faible dose qu’à forte dose, et qu’il faut donc le tester avec des doses suffisamment faibles pour révéler ses dangers.
Je dois avouer qu’en lisant cela, j’ai clairement pensé que c’était n’importe quoi. Comment un poison peut-il être plus dangereux quand sa dose diminue ? Sauf à croire à un effet homéopathique, bien sûr. Et pourtant, après m’être un peu documenté, il semble bien que ce type d’effets puisse exister, et soit en train de bouleverser les conceptions traditionnelles en matière de toxicologie et de sécurité sanitaire.
 Les fondements de la toxicologie
Les fondements de la toxicologie
« Tout est mortel. Rien n’est mortel. C’est juste question de quantité. »
C’est avec cette formule simple que le médecin/alchimiste Paracelse a jeté au XVIème siècle les bases de la toxicologie. Derrière cette vision se cache un principe frappé au coin du bon sens : quand la dose augmente, les dangers d’un poison augmentent (ou au pire stagnent).
Cette idée en apparence incontestable est d’ailleurs toujours à la base des principes de sécurité sanitaire : pour s’assurer de l’absence de risques liés à une substance, on la teste à différente doses, et quand on identifie une dose sans effet majeur pour la santé, on considère qu’on est tranquilles tant que l’on reste en-dessous.
Voilà qui est parfait, mais qui repose sur l’idée que la toxicité d’une substance ne peut que diminuer quand la dose diminue. Malheureusement, on trouve de plus en plus de contre-exemples à ce principe.
Les courbes de toxicité non-monotones
Dans les études de toxicologie, on mesure généralement ce qu’on appelle des courbes dose / réponse. Cela consiste à prendre quelques malheureux cobayes animaux, et à leur administrer différentes doses du produit que l’on étudie. On mesure alors une réponse, qui peut être le poids de l’animal, le nombre ou la taille de tumeurs cancéreuses, un degré d’inflammation, etc.
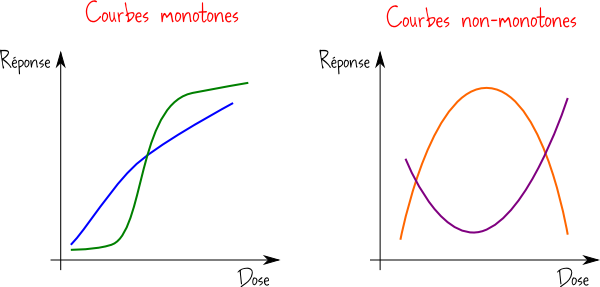
Dans les cas traditionnels, l’effet augmente ou stagne avec la dose, et on obtient ce qu’on appelle une courbe dose-réponse monotone. Mais depuis maintenant plusieurs années, les toxicologues ont remarqué que certaines substances possèdent des courbes dont le sens peut soudainement changer. On peut ainsi trouver des courbes en forme de U, de U inversé ou même des choses plus compliquées. On parle de courbes non-monotones. Le schéma ci-dessous illustre la différence entre les deux.
Les perturbateurs endrocriniens
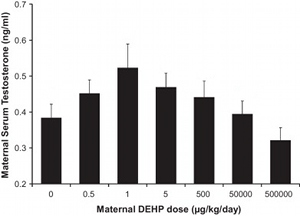 Bien que les substances provoquant des courbes de toxicité non-monotones ne soient pas légion, cela fait maintenant plus d’une dizaine d’années que des travaux sont publiés régulièrement avec ce type de résultats. La courbe ci-contre en montre un exemple spectaculaire [1]. Le produit considéré est le di-(2-ethylhexyl)-phthalate (DEHP pour les intimes), un plastifiant utilisé notamment dans la fabrication du PVC.
Bien que les substances provoquant des courbes de toxicité non-monotones ne soient pas légion, cela fait maintenant plus d’une dizaine d’années que des travaux sont publiés régulièrement avec ce type de résultats. La courbe ci-contre en montre un exemple spectaculaire [1]. Le produit considéré est le di-(2-ethylhexyl)-phthalate (DEHP pour les intimes), un plastifiant utilisé notamment dans la fabrication du PVC.
Dans l’expérience considérée, du DEHP a été administré à diverses doses à des souris enceintes, et le niveau de testosterone dans le serum sanguin a été mesuré à un moment donné de la grossesse. Comme vous pouvez les voir sur le graphique ci-contre, les doses vont de 0.5 à 500 000 microgrammes par jour et par kilogramme de poids corporel. Entre la plus forte et la plus faible dose testée, il y a donc un facteur 1 million ! Et de manière surprenante, la réponse maximale est observée pour une des doses les plus faibles.
Le cas du DEHP n’est malheureusement pas isolé. De nombreux résultats analogues ont été publiés, et la quasi-totalité concerne ces substances que l’on qualifie de perturbateurs endocriniens. Il s’agit de molécules qui peuvent se lier à certains récepteurs normalement réservés aux hormones, et ainsi perturber le bon équilibre de notre organisme. Le bisphénol A est bien sûr soupçonné d’appartenir à cette catégorie, tout comme l’atrazine ou le triclosan, des produits chimiques utilisés comme pesticides.
Tout cela peut-il être vrai ?
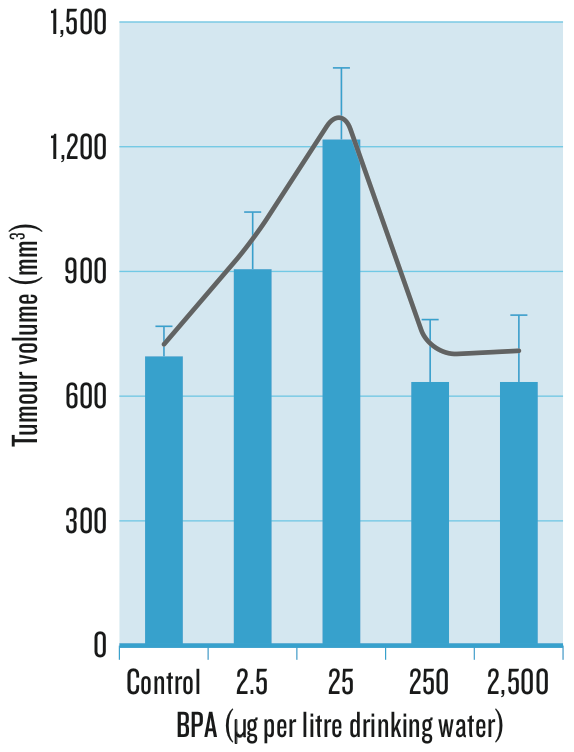 Malgré les publications scientifiques allant dans ce sens, l’existence de courbes dose-réponse non-monotones peut paraître difficile à admettre. Qu’un produit perturbateur endocrinien puisse avoir un effet à très faible dose, cela paraît tout-à-fait possible. Mais que l’effet puisse diminuer quand la dose augmente, est-ce bien réaliste ? (ci-contre, une des courbes publiées pour le bisphénol A [2]).
Malgré les publications scientifiques allant dans ce sens, l’existence de courbes dose-réponse non-monotones peut paraître difficile à admettre. Qu’un produit perturbateur endocrinien puisse avoir un effet à très faible dose, cela paraît tout-à-fait possible. Mais que l’effet puisse diminuer quand la dose augmente, est-ce bien réaliste ? (ci-contre, une des courbes publiées pour le bisphénol A [2]).
Comme souvent en sciences, une affirmation extraordinaire requiert des preuves extraordinaires : on peut donc comprendre que l’idée ne fasse pas encore consensus dans la communauté des toxicologues. Et ce d’autant que la plupart des publications sur le sujet sont l’œuvre d’une seule et même équipe : celle de Frederick Vom Saal à l’université du Missouri, qui en a fait son fond de commerce. Pour ma part, je trouve les effets quand même faibles par rapport aux barres d’erreur.
Et pourtant, si l’on réfléchit bien, il n’y a rien d’étonnant à ce que des courbes non-monotones existent. Pensez au sel pour votre organisme : il est indispensable à faible dose, mais dangereux à forte dose. Sa courbe dose-réponse est donc en U inversé (et c’est d’ailleurs pour cela que le goût salé à faible dose est agréable, mais désagréable en trop grande quantité : notre organisme sait qu’il existe un optimum !). Et cet argument peut se décliner pour la quasi-totalité des nutriments indispensables à notre organisme.
Malgré tout, il faut reconnaitre que l’on manque de preuves pour expliquer les mécanismes qui pourraient expliquer les courbes non-monotones des perturbateurs endocriniens. Toutefois avec certains médicaments, on a déjà observé de tels effets. Ainsi le tamoxifen, utilisé contre certains cancers, a une courbe de réponse non-monotone [2] : à trop faible dose il stimule la tumeur, et l’on doit en administrer une dose suffisante pour qu’il agisse contre les cellules cancéreuses. Des chercheurs ont pu relier cet effet au fait que cette molécule stimule l’expression de certains gènes à faible dose, mais l’inhibe à forte dose.
Malgré ces premiers éléments, attester fermement l’existence de courbes dose-réponse non-monotones, et expliquer les mécanismes impliqués, est encore un travail de longue haleine. Une grosse étude est d’ailleurs en cours sur le bisphénol A, prévoyant de tester des doses variant de 1 à 100 000, afin de trancher définitivement la question.
Billets reliés :
Sur les plastiques, et ce qu’est le bisphénol A : un plastique fantastique
Un autre problème de toxicologie et santé publique : Faut-il avoir peur des nanoparticules ?
Références :
A ce jour depuis un an, Le Monde a publié 53 articles contenant le terme « bisphenol » (enfin pas mal d’articles sortent en double…)
[1] Do, Rylee Phuong, et al. « Non-monotonic dose effects of in utero exposure to di (2-ethylhexyl) phthalate (DEHP) on testicular and serum testosterone and anogenital distance in male mouse fetuses. » Reproductive Toxicology (2012).
[2] Dan Fagin, News Feature. Toxicology : the learning curve, Nature 490 2012





Comments
Il semble que ce phénomène ait été identifié vis à vis des abeilles ds les années 90 avec le Gaucho – un insecticide systémique produit par Bayer-. D’après les tests de toxicité effectués par le fabricant cet insecticide n’affectait pas les abeilles mais on a constaté ensuite que les restes subsistant ds le sol entrainaient une forte mortalité l’année suivante pr les abeilles butinant sur les parcelles traitées.
Pingback: Le bisphénol A peut-il être plus t...
Bonjour, je trouve contestable l’argument sur le sel.
Il ne faut pas confondre la toxicité et la carence.
À faible dose, le sel n’est pas toxique, c’est son absence qui empêche le bon fonctionnement du corps qui en a besoin.
Il faut bien préciser qu’on parle de la toxicité de la substance, c’est-à-dire du mal qu’elle fait.
Sur le bisphénol A, c’est autre chose, puisque ce n’est pas une substance nécessaire au fonctionnement du corps humain.
—–
Et en espérant passer cette fois à côté des insultes,
un petit s à supprimer dans la partie « Les fondements de la toxicologie » (partie en gras) :
« quand on identifie une dose […], on considère qu’on est tranquilleS tant que […] »
—–
Bien cordialement
JC Salmon, qui apprécie toujours la qualité de vos articles,
et admire votre capacité à rédiger des articles clairs et de haut niveau dans des domaines scientifiques différents.
Je trouve l’exemple de la vitamine A plus probant. La carence en vitamine A rend aveugle. Une forte dose est un poison mortel qui a provoqué la mort de l’explorateur Xavier Mertz qui avait mangé ses chiens de traîneau.
Non, c’est exactement pareil. C’est la carence en vitamine A qui est toxique et non sa présence.
On ne peut donc pas dire que la vitamine A est toxique à faible dose.
Pingback: Le bisphénol A peut-il être plus t...
Bonjour,
C’est un effet identifié déjà depuis la fin du 19 ième siècle, appelé hormèse ou effet hormesis (http://fr.wikipedia.org/wiki/Horm%C3%A8se).
Le plus spectaculaire et plus controversé aspect de l’hormèse à mon avis est celui des faibles doses de radioactivité qui s’avèrent bénéfiques selon la littérature scientifique (en particulier sur les cancers), à l’exception à ma connaissance du radon, pour lequel il existe une relation linéaire entre la dose reçu et le risque de cancer du poumon bien documenté sur le plan scientifique.
Voir à ce sujet un rapport de l’académie des sciences et de médecine par Tubiana et Aurengo : « La relation dose-effet et l’estimation des effets cancérogènes des faibles doses de
rayonnements ionisants » http://www.academie-sciences.fr/activite/rapport/rapport070405.pdf
On trouve quelques études spectaculaires sur ces questions,en particulier celle-ci : http://www.jpands.org/vol9no1/chen.pdf à lire attentivement…
Attention, c’est un point de vue absolument pas politiquement correct, en ces temps d’irrationalité collective à la limite du délire sur les menaces imaginaires multiples qui nous assaillent de toutes part et porterait atteinte à notre santé !
Un sujet à creuser pour un prochain article 😉
Merci pour la qualité de ceux-ci et de votre blog.
Oups ! l’hormèse (faible doses bénéfique et fortes toxiques), c’est bien sûr le contraire de l’effet ici discuté, ou les faibles doses sont toxiques alors que les fortes ne le sont pas. Un autre exemple de courbe non monotone donc.
Bonjour
Je trouve aussi l’exemple du sel tiré par les cheveux. Et même non adapté du tout. En effet, la courbe en U du sel n’est pas celle de sa toxicité (c’est celle de rien du tout). Comme expliqué par JC Salmon, le sel n’est pas toxique à basse concentration. Il a donc une courbe plus ou moins linéaire de toxicité. Sinon sujet intéressant mais malheureusement le fait que toutes les etudes faites à ce sujet sont faites par le même labo arrive un peu tard dans l’article car on se rend compte que ça discredite l’ensemble du propos. Même si comme je l’ai dit, l’idée est loin d’etre idiote. Ca quand même de fondations solides sur l’argumentaire (d’autres travaux menés s’il en existe etc). Merci.
Ça manque *
En fait mon exemple sur le sel n’était pas là pour donner un exemple de « toxicité non-linéaire », mais plutôt pour montrer qu’en général, une « réponse non-linéaire » n’avait rien d’inconcevable. J’aurai pu aussi bien prendre l’eau comme exemple (ou le sexe…)
C’est bien dans ce sens que j’ai cité la vitamine A qui m’avait particulièrement frappé quand j’en ai entendu parler.
Je reviens sur ce que dit Marco,
que ce soit le sel, l’eau, le sexe ou la vitamine A, c’est exactement la même chose.
Il faudrait envisager deux courbes, qu’on peut imaginer droites pour simplifier :
toxicité en fonction de la quantité absorbée par unité de temps
nocivité de la carence en fonction de la quantité absorbée par unité de temps.
Et les effets nocifs s’obtiendraient en ajoutant les deux fonctions.
On obtiendrait bien une courbe en U, mais qui ne correspond pas à la toxicité de la substance.
L’homéopathie est un exemple plus parlant, avec une réelle toxicité à (plus que très) basse concentration et à haute concentration. [Qu’on croie ou non à l’homéopathie n’est pas le sujet]
Et il y a fort à parier que la très grande majorité des substances aient ces effets :
Le sucre, l’huile, le soleil, l’oxygène, la confiance en soi, le besoin de bouger…
Je pense qu’il faudrait s’intéresser aux substances dont le corps n’a pas besoin,
et dont les effets d’une basse concentration ne soit pas une carence :
la radioactivité (comme dans l’article), les antibiotiques, le savon, l’essence, le cannabis, les somnifères…
Hello, hello,
Je me permets de m’immiscier dans cette discussion mais loin de moi l’idée d’être scientifique :
Est-ce qu’une faible dose pourrait passer sous le radar alors qu’une plus forte déclenche un système de défense ?
L’exemple connu de la grenouille qu’on fait bouillir n’est pas parfait mais illustre un peu l’idée. A feu doux elle n’y voit que du feu et se laisse bouillir mais plongez-la dans l’eau bouillante et elle voudra ressortir en gémissant.
On pourrait alors remplacer la notion de :
_ « concentration du principe actif » par la notion « de vitesse de variation de température » ou « différence de température »
_ »résistance au poison » par la « réaction de survie de la bestiole »
——————-
Autre exemple :
Je me souviens d’un cours de T S il y a 17ans, (en fait dire « me souvenir » est un peu exagéré) et la prof nous montrait une expérience qu’elle avait préparé avec de la limaille de fer (si je me souviens bien) dans laquelle elle versait au goutte à goutte un produit qui était censé créer une réaction exothermique et un changement de coloration de toute sa limaille (si je me souviens bien). Bien sûr son expérience n’a pas fonctionné (je m’en souviens bien mdr) et seule une partie de sa limaille avait changé de couleur. (Si je me souviens bien) elle avait considéré comme hypothèse que sa solution était possiblement trop concentré ce qui aurait agi instantanément avec la limaille mais créant ainsi une barrière physique (d’oxydation ?) qui empêchait que la solution se propage à travers tout l’échantillon. Ainsi une solution moins concentrée aurait pu plus se répartir dans la limaille et faire réagir toute celle-ci mais de manière plus lente.
Je laisse ces exemples à vos critiques constructives car il est peu probable qu’ils soient d’un intérêt à votre article, et ainsi je comprendrai mieux mes erreurs d’interprétation et de logique.
Toujours un plaisir de vous lire,
Cordialement,